1 Lomas A, Leonardi-Bee J, Bath-Hextall F. A systematic review of worldwide incidence of nonmelanoma skin cancer. Br J Dermatol. 2012;166:1069–80.
2 Chinem VP, Miot HA. Epidemiology of basal cell carcinoma. Ann Bras Dermatol. 2011;86:292–305.
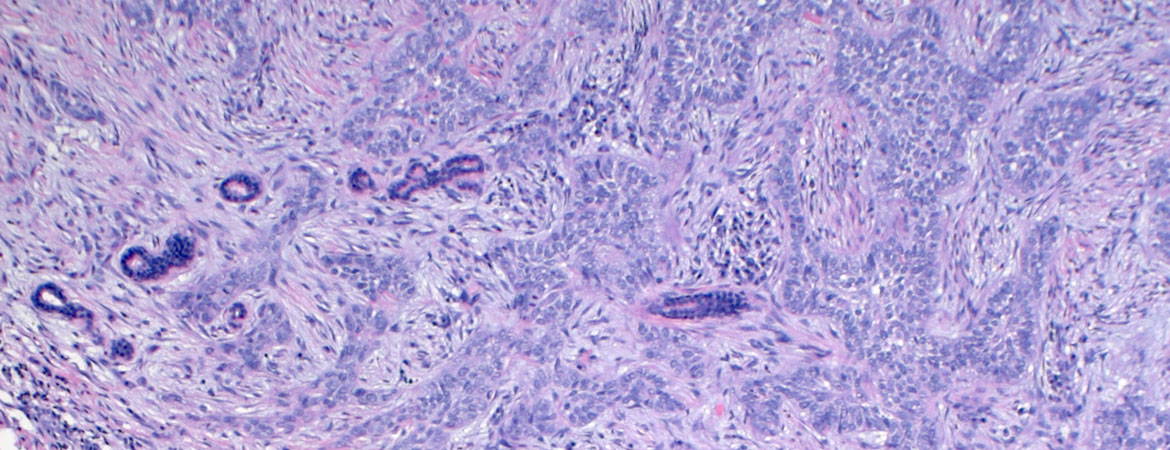
3 Rubin AI, Chen EH, Ratner D. Basal-Cell Carcinoma. N Engl J Med. 2005;353:2262–9.
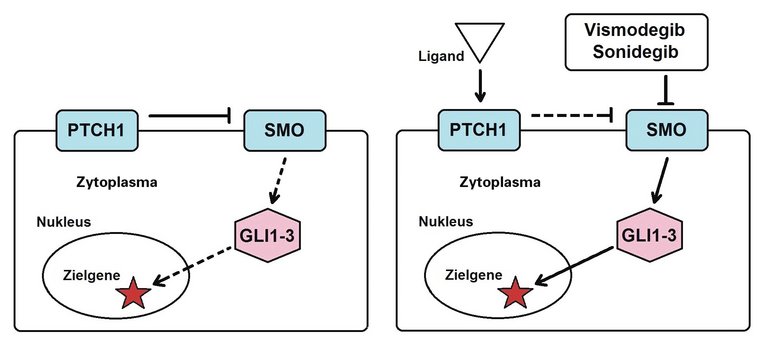
4 Von Hoff DD, Lo Russo PM, Rudin CM, Reddy JC et al. Inhibition of the hedgehog pathway in advanced basal-cell-carcinoma, N Engl J Med. 2009;361:1164–72.
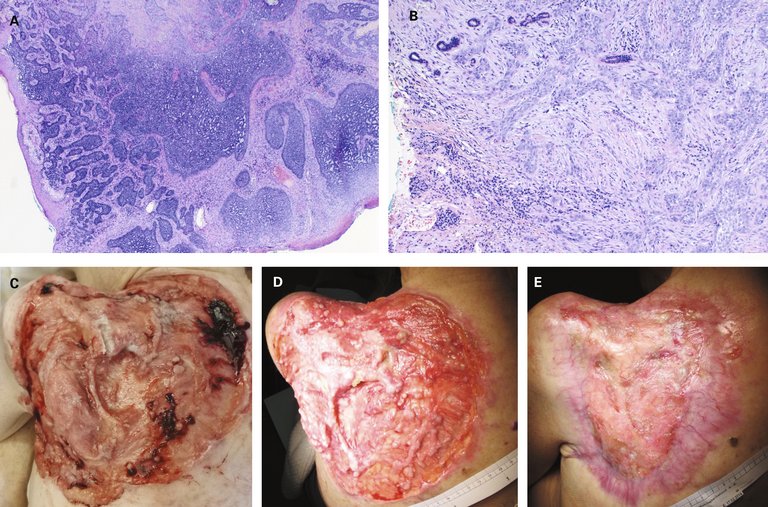
5 Sekulic A, Migden MR, Oro AE, Dirix L et al. Efficacy and safety of Vismodegib in Advanced Basal-Cell Carcinoma. N Engl J Med. 2012;366:2171–9.
6 Sekulic A, Migden MR, Lewis K, Hainsworth JD et al. Pivotal Erivance basal cell carcinoma study: 12-month update of efficacy and safety of vismodegid in advanced BCC. J Am Acad Dermatol. 2015;72:1021–6.
7 Sekulic A, Migden MR, Basset-Seguin N, Garbe C et al. Long-term safety and efficacy of vismodegib in patients with advanced basal cell carcinoma (aBCC): 24-month update of the pivotal ERIVANCE BCC study. JAAD 2014;70(5):AB137 (Supplement 1).
8 Mohan SV, Chang J, Li S, Henry AS et al. Increased risk of cutaneous squamous cell carcinoma after vismodegib therapy for basal cell carcinoma. JAMA Dermatol. 2016;152:527–32.
9 Basset-Seguin N, Hauschild A, Grob JJ, Kunstfeld R et al. Vismodegib in patients with advanced basal cell carcinoma (STEVIE): a pre-planned intermin analysis of an international open-label trial. Lancet Oncol. 2015;16:279–36.
10 Dréno B, Kunstfeld R, Hauschild A, Fosko S et al. Two intermittent vismodegib dosing regimens in patients with multiple basal-cell carcinomas (MIKIE): a randomised, regimen-controlled, double-blind, phase 2 trial. Lancet Oncol. 2017; 18(3):404–12.
11 Malhi V, Colburn D, Williams SJ, Hop CE et al. A clinical drug-drug interaction study to evaluate the effect of a proton-pump inhibitor, a combined P-glycoprotein/cytochrome 450 enzyme (CYP)3A4 inhibitor, and a CYP2C9 inhibitor on the pharmacokinetics of vismodegib. Cancer Chemother Pharmacol. 2016;78:41–9.
12 Migden MR, Guminski A, Gutzmer R, Dirix L et al. Treatment with two different doses of sonidegib in patients with locally advanced or metastatic basal cell carcinoma (BOLT): a multicentre, randomised, double-blind phase 2 trial. Lancet Oncol. 2015;16:716–28.
13 Dummer R, Guminski A, Gutzmer R, Dirix L et al. The 12-month analysis from basal cell carcinoma outcomes with LDE225 treatment (BOLT): a phase II, randomized, double-blind study of sonidegib in patients with advanced basal cell carcinoma. J Am Acad Dermatol. 2016;75:113–25.
14 Kim DJ, Kim J, Spaunhurst K, Montoya J et al. Open-label exploratory phase II trial of oral Itraconazole for the treatment of basal cell carcinoma. J Clin Oncol. 2014;32:745–51.
15 Chen B, Trang V, Lee A, Williams NS et al. Posaconazole, a second-generation triazole antifungal drug, inhibits the hedgehog signaling pathway and progression of basal cell carcinoma. Mol Cancer Ther. 2016;15:866–7.
– Dummer R, Guminski A, Gutzmer R, Dirix L et al. The 12-month analysis from basal cell carcinoma outcomes with LDE225 treatment (BOLT): a phase II, randomized, double-blind study of sonidegib in patients with advanced basal cell carcinoma. J Am Acad Dermatol. 2016;75:113–25.
– Rubin AI, Chen EH, Ratner D. Basal-Cell Carcinoma. N Engl J Med. 2005;353:2262–9.
– Von Hoff DD, Lo Russo PM, Rudin CM, Reddy JC et al. Inhibition of the hedgehog pathway in advanced basal-cell-carcinoma, N Engl J Med. 2009;361:1164–72.
– Sekulic A, Migden MR, Oro AE, Dirix L et al. Efficacy and safety of Vismodegib in Advanced Basal-Cell Carcinoma. N Engl J Med. 2012;366:2171–9.
– Dréno B, Kunstfeld R, Hauschild A, Fosko S et al. Two intermittent vismodegib dosing regimens in patients with multiple basal-cell carcinomas (MIKIE): a randomised, regimen-controlled, double-blind, phase 2 trial. Lancet Oncol. 2017;18(3):404–12.