EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 44
support@swisshealthweb.ch
www.swisshealthweb.ch
Publiziert am 01.01.2022
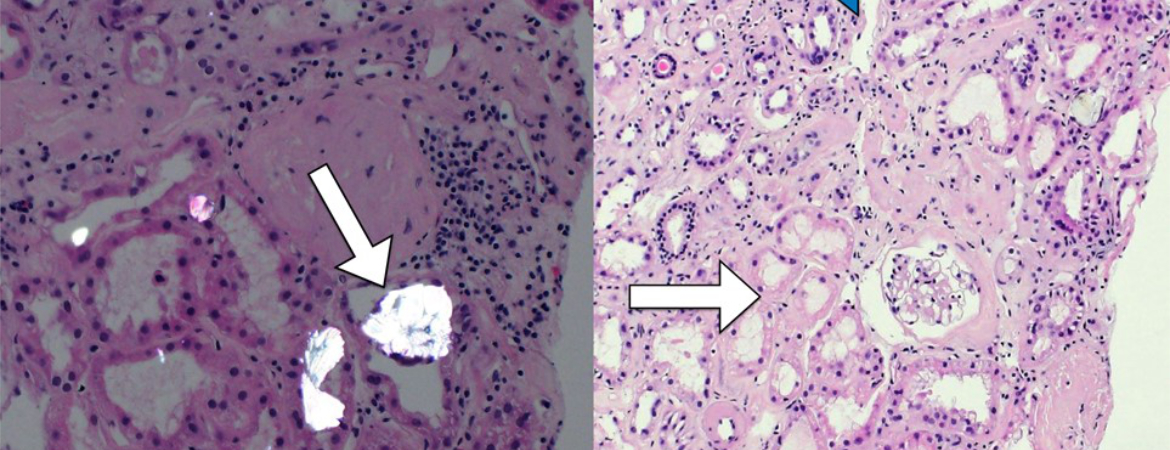
Ein 71-jähriger Patient wurde mit akutem Nierenversagen und seit über einer Woche bestehender Übelkeit mit Erbrechen sowie Diarrhoe aus einer Rehabilitationsklinik zugewiesen.
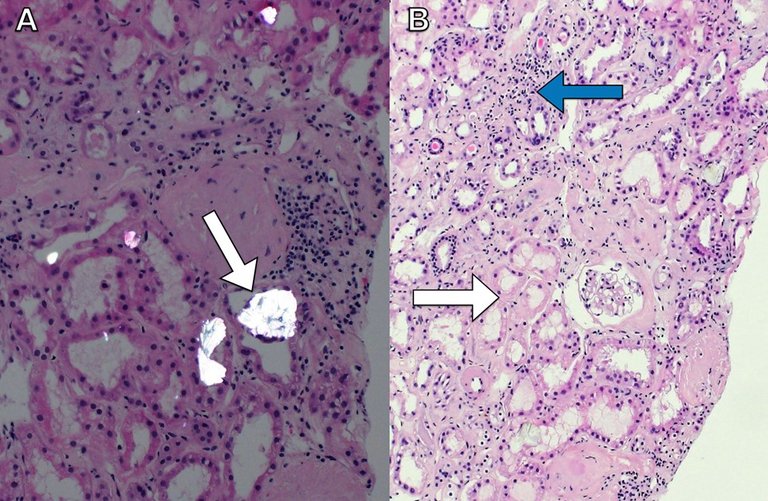
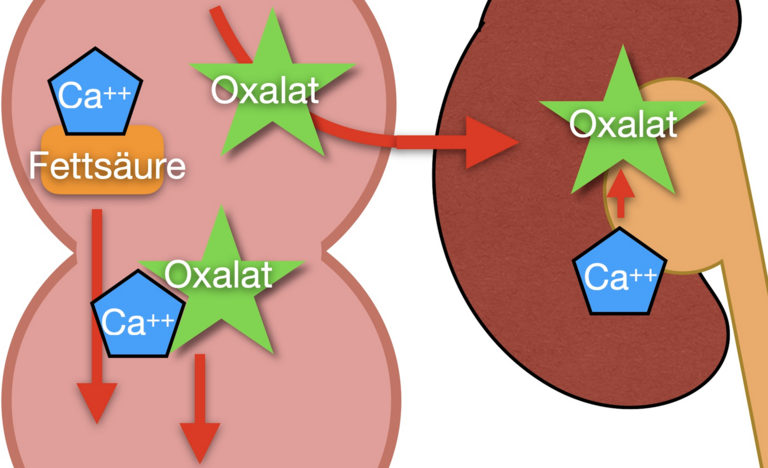
| Therapie | Dosierung | Ziel | Referenz |
| Volumengabe | individuell, bis 3L/1.73m2/d | Reduktion tubuläre Oxalatkonzentration | 1, 12 |
| Calcium Substitution | min. 1000mg / Tag p.o. | Oxalatbindung im Darm | 13 |
| Citrat Substitution | z.B. Kaliumcitrat 3-6 g/d p.o. | Reduktion Nierensteinbildung | 14 |
| Oxalat-arme Diät: keine Schokolade, Tee, Spinat, Rhabarber | Reduktion intestinales Oxalataufkommen | 12 | |
| Pankreasenzyme | individuell, abhängig von Fettgehalt und Symptomatik 25 000 – 80 000 E pro Mahlzeit | Reduktion Oxalatabsorption bei exokriner Pankreasinsuffizienz | 1 |
Veröffentlicht unter der Copyright-Lizenz.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Keine kommerzielle Weiterverwendung ohne Genehmigung.
See: emh.ch/en/emh/rights-and-licences/