EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 44
support@swisshealthweb.ch
www.swisshealthweb.ch
Publiziert am 25.09.2019
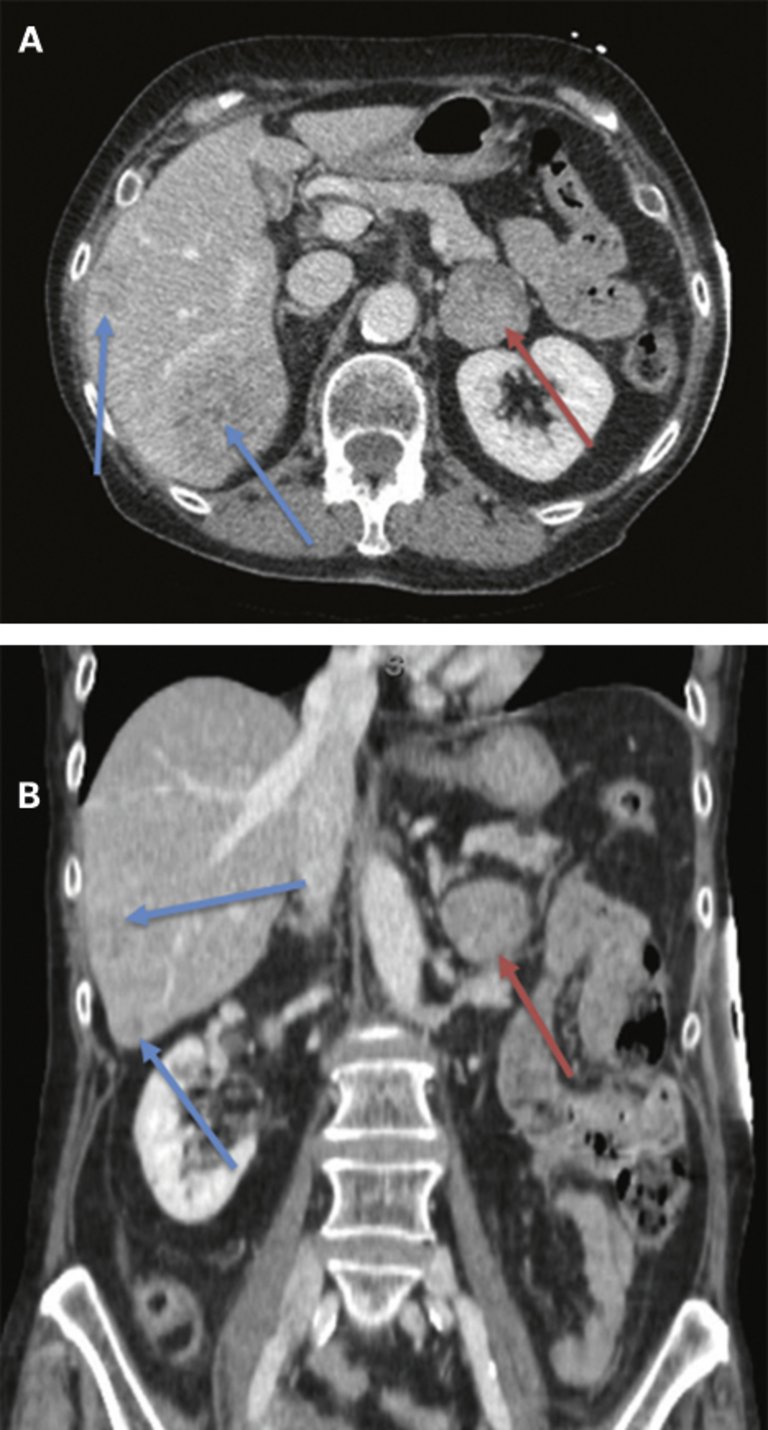
Die aufgrund eines lobulären invasiven mit Mastektomie und Hormontherapie behandelten Mammakarzinoms der linken Brust vorbekannte Patientin kommt aufgrund von Asthenie, Verwirrung und Gewichtszunahme in die Notaufnahme.
| Tabelle 1: Ursachen für endogenen Hyperkortisolismus (angepasst nach [5]). | |
| Häufigkeit | |
| ACTH-abhängig | 70–80% |
| Cushing-Syndrom (hypophysäre Ursache) • Kortikotropes Adenom • Kortikotrope Hyperplasie | 60–70% |
| Ektope ACTH-Bildung
(nicht-hypophysäre Ursache) • Gutartige neuroendokrine Tumoren • Bösartige neuroendokrine Tumoren • Okkulte neuroendokrine Tumoren | 5–10% |
| ACTH-unabhängig (adrenal) | 20–30% |
| Nebennierenadenome | 10–20% |
| Bösartige Nebennierenrindenkarzinome | 5–7% |
| Nebennierenhyperplasien | <4% |


Veröffentlicht unter der Copyright-Lizenz.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Keine kommerzielle Weiterverwendung ohne Genehmigung.
See: emh.ch/en/emh/rights-and-licences/