EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 44
support@swisshealthweb.ch
www.swisshealthweb.ch
Publié le 18.12.2019
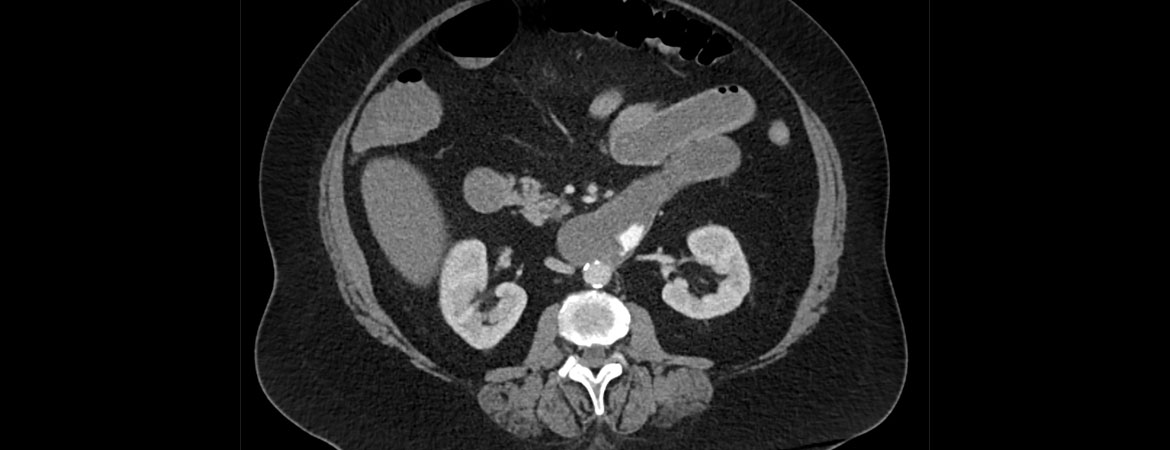
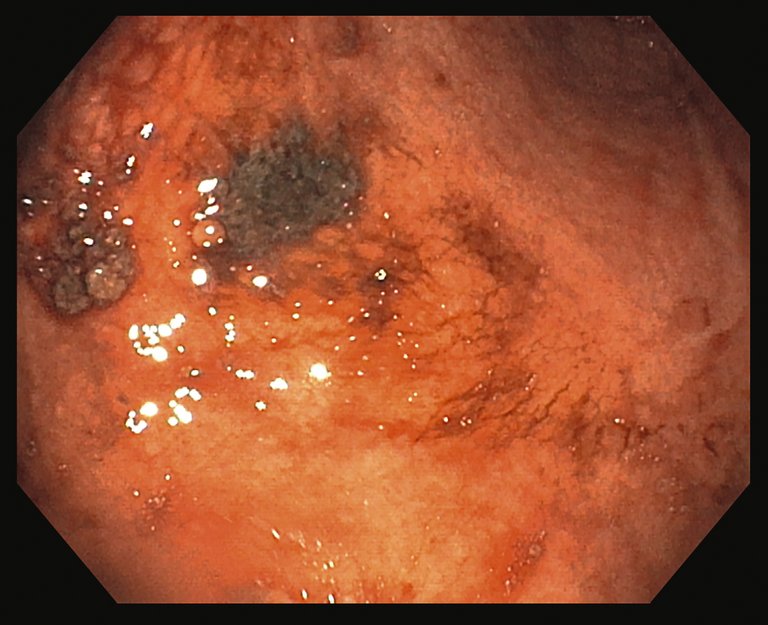
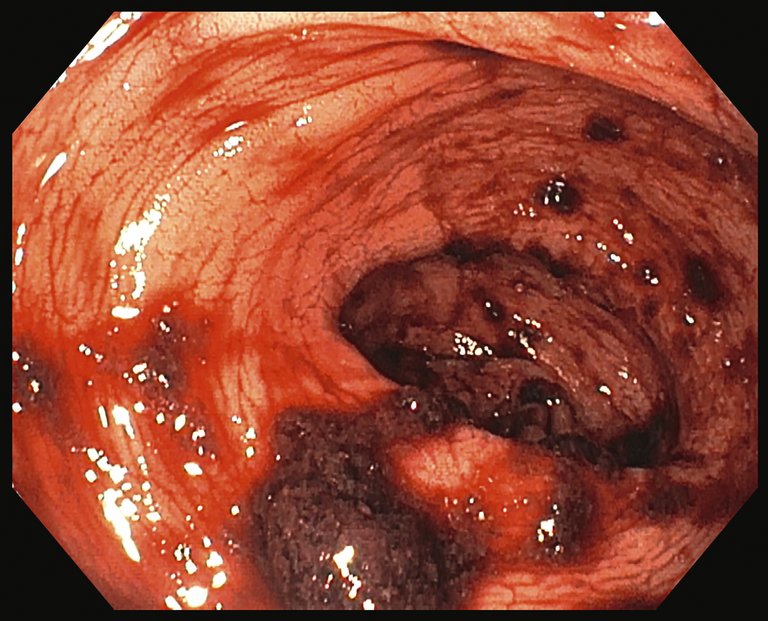
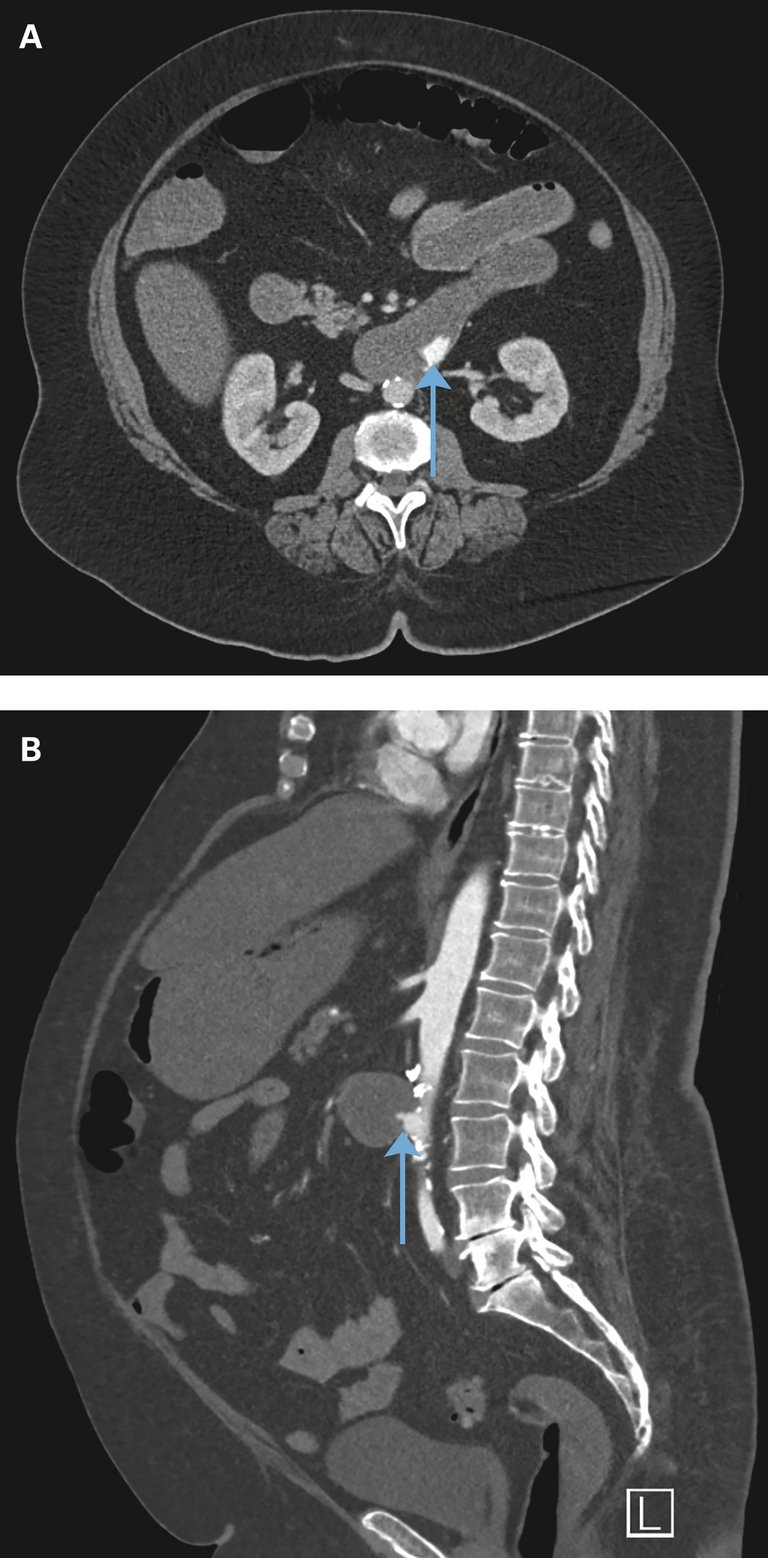
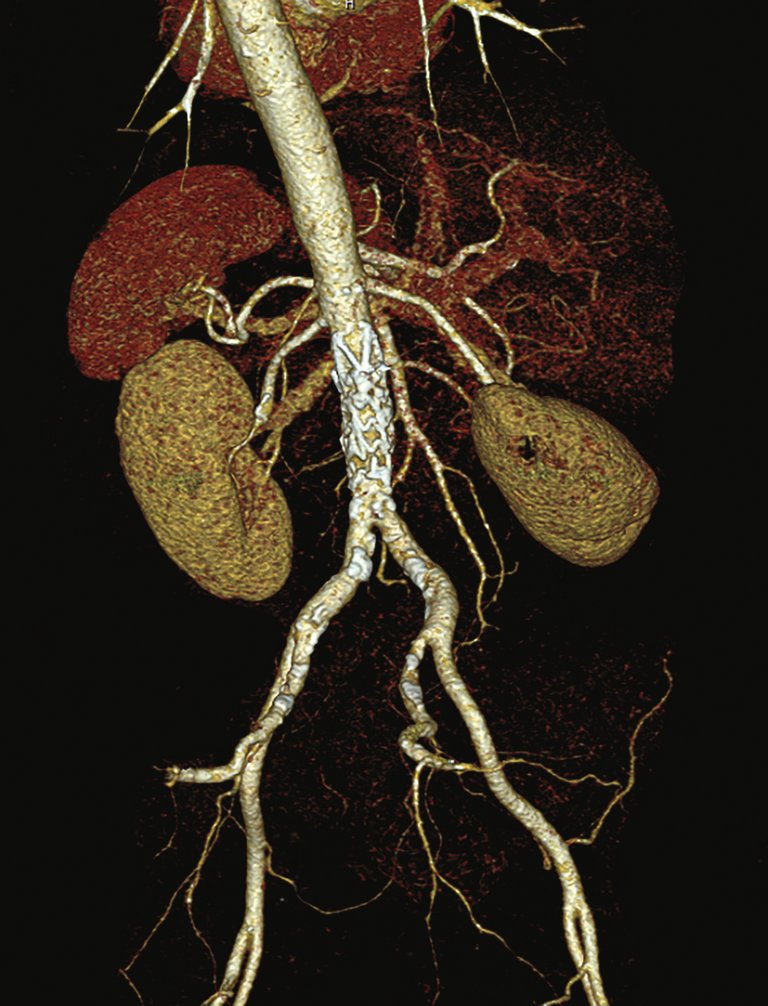
Une patiente âgée de 64 ans a été conduite dans le service des urgences par les secours en raison d’une hématochézie ainsi que d’une tachycardie croissante et d’une diminution de l’état général.
Publié sous la licence du droit d'auteur.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Pas de réutilisation commerciale sans autorisation..
See: emh.ch/en/emh/rights-and-licences/