EMH Schweizerischer Ärzteverlag AG
Farnsburgerstrasse 8
CH-4132 Muttenz
+41 (0)61 467 85 44
support@swisshealthweb.ch
www.swisshealthweb.ch

Publié le 05.07.2022
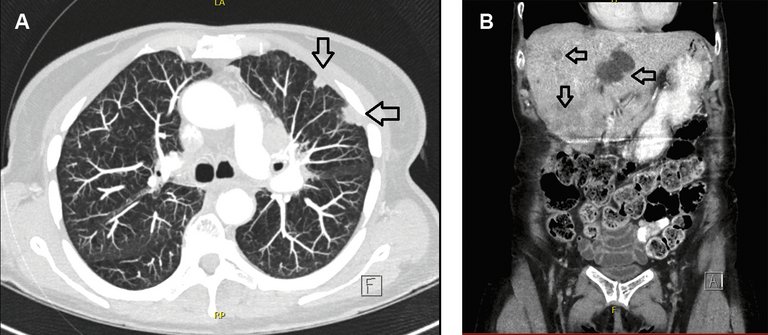
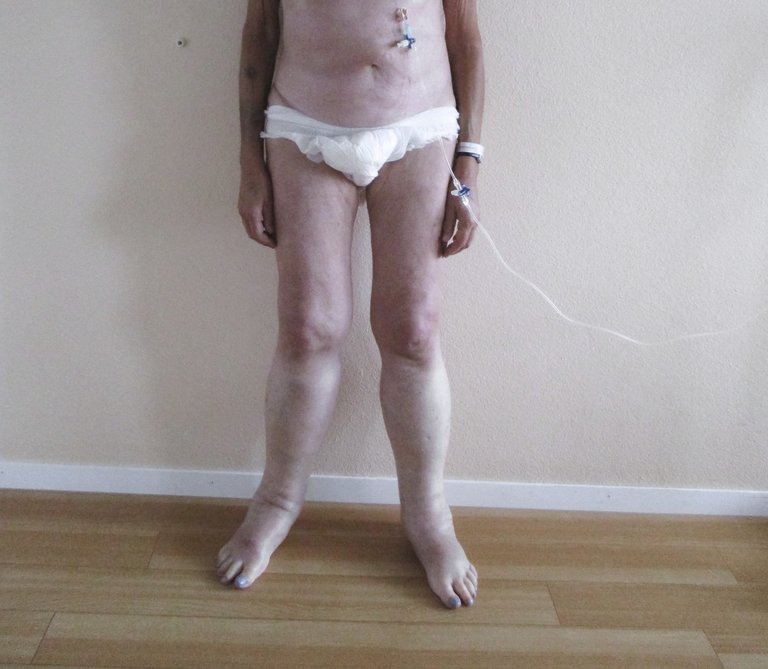
Présentation d’une patiente de 63 ans qui, en plus d’une faiblesse prédominante au niveau des jambes, avait des œdèmes croissants au niveau des jambes ainsi qu’un ralentissement général.
| Tableau 1: Résultats de laboratoire à l’admission. | ||
| Jour d’admission | Valeurs de référence | |
| Sodium (mmol/l) | 133 | 135–145 |
| Potassium (mmol/l) | 1,8 | 3,5–4,8 |
| Créatinine (µmol/l) | 35 | 44–80 |
| Débit de filtration glomérulaire (ml/min/1,73m2) | 111 | |
| Glucose (mmol/l) | 6.7 | 4,6–6,4 |
| Protéine C-réactive (mg/l) | 6,3 | <5,0 |
| Leucocytes (103/µl) | 11,0 | 3,7–11,2 |
| Cortisol (nmol/l) | 1338 | |
| Gazométrie veineuse | ||
| pH | 7,56 | 7,35–7,45 |
| pO2 (mm Hg) | 57,7 | |
| pCO2 (mm Hg) | 26,7 | |
| Bicarbonate (mmol/l) | 52,5 | 21–26 |
| Chlorure (mmol/l) | 68 | 98–106 |

| Tableau 2: Aperçu des options thérapeutiques médicamenteuses du syndrome de Cushing ectopique paranéoplasique. | |||
| Inhibiteurs de la stéroïdogenèse | |||
| Mode d’action | Avantage | Inconvénient | |
| Métyrapone | Inhibiteur de la 11-β-hydroxylase | Début d’action rapide | Accumulation de précurseurs des minéralocorticoïdes qui agissent également sur le récepteur des minéralocorticoïdes |
| Kétoconazole | Inhibiteur de la stéroïdogenèse (inhibition de la cholestérol-20,22-desmolase et de la 11-bêta-hydroxylase), antimycosique | Utilisation la plus répandue et la plus éprouvée | Hépatotoxicité, inhibition du CYP3A4 |
| Mitotane | Cytostatique et adrénostatique | Effet cytostatique simultané en cas de carcinome corticosurrénalien | Début d’action lent, profil d’effets indésirables neurologiques et gastro-intestinaux |
| Etomidate | Anesthésique injectable et adrénostatique | Seul médicament pouvant être administré par voie intraveineuse | En cas de sédation, une prise en charge en soins intensifs est nécessaire, donc adapté comme solution transitoire |
| Osilodrostat | Inhibiteur de la stéroïde-18-hydroxylase et de la 11-β-hydroxylase | - | Accumulation de précurseurs des minéralocorticoïdes qui agissent également sur le récepteur des minéralocorticoïdes |
| Antagonistes des récepteurs des glucocorticoïdes | |||
| Mifépristone | Antagoniste des récepteurs des glucocorticoïdes et de la progestérone | - | Surveillance compliquée du fait d’une augmentation de l’ACTH et du cortisol |
Publié sous la licence du droit d'auteur.
"Attribution - Non-Commercial - NoDerivatives 4.0"
Pas de réutilisation commerciale sans autorisation..
See: emh.ch/en/emh/rights-and-licences/